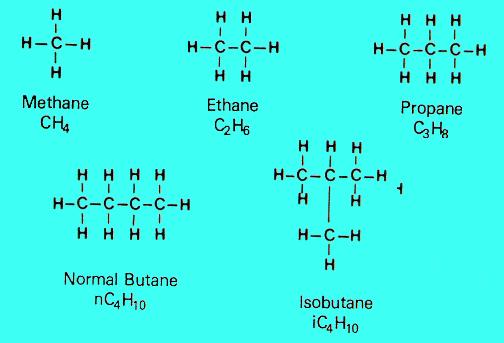
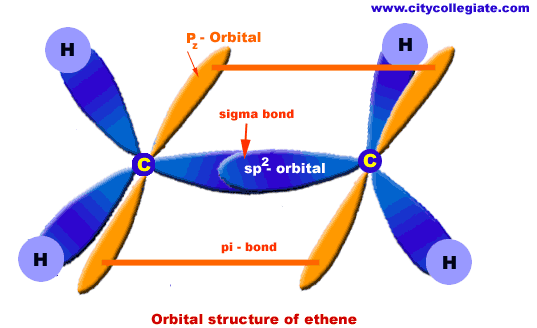
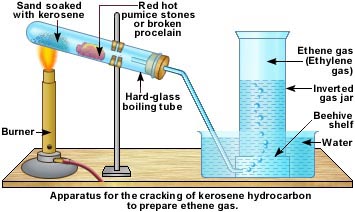
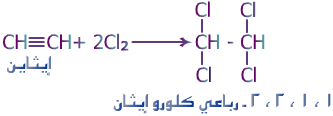
الأحماض الكربوكسيلية
تعتبر الاحماض الكربوكسيلية من أهم الاحماض العضوية من حيث وجودها واستخداماتها,
.cooh وتتميز بوجود المجموعة الوظيفية المسماة كربوكسيل
التسمية:
- للكثير منها أسماء شائعة.
- يرمز للحمض في نظام أيوباك بالنهاية "ويك" التي تلحق باسم الالكان مع اضافة كلمة حمض, ch3ch2cooh مثل: حمض بروبانوك
التحضير:
- من التحلل المائي للزيوت والدهون والنيتريلات.
- من أكسدة الكحولات الأولية, والالدهيدات, وبعض الالكينات, ومجموعات الالكيل المتصلة بحلقة البنزين.
للاحماض الكربوكسيلية القدرة على انشاء روابط هيدروجينية مع نفسها ومع الماء, مما يجعل درجات غليانها وذوبانها أكثر من الايثرات والكحولات والالدهيدات المتقاربة منها في أوزانها الجزيئية.
للاحماض الكربوكسيلية تفاعلات حمضية, حيث تكون أملاحا مع القلويات .
وتعزى زيادة الخاصية الحمضية لمجموعة الهيدروكسيل للأحماض عنها في الكحولات الى تأثير مجموعة الكربونيل التي ترتبط بها.
تتأين الأحماض الكربوكسيلية في أغلب الأحيان في المحلول في المحلول المائي بدرجة قليلة, وهي أحماض ضعيفة, تقل قوتها بدرجة كبيرة عن الأحماض المعدنية.
تتفاعل الأحماض الكربوكسيلية مع الكحولات في وجود مادة متنوعة للماء, لتعطي الاسترات المقابلة.
الأحماض العضوية فى حياتنا
الحمض الصيغة المصدر الإستخدام
حمض الفورميك HCHO يفرزة النمل الأحمر دفاعا عن نفسة ويستخدم فى صناعة الصبغات والمبيدات الحشرية والعطور والعقاقير والبلاستيك
حمض الأسيتيك CH3COOH -الحمض النقى (100 % ) سائل عديم اللون
-لة تأثير كاوي على الجلد -لة رائحة نفاذة
-يتجمد عند 16 درجة مئوية إلى مادة صلبة تشبة الثلج -الحمض الثلجــي :هو الحمض النقى ذو التركيز 100% يستخدم
1- بتركيز 4% على هيئة خل
2-تحضير الحرير الصناعى والصبغات والمبيدات الحشرية و والاضافات الغذائية
حمض بنزويك
شحيح الذوبان فى الماء ولذا يحول إلى الملح الصوديومى او البوتاسيومى ليكون قابلا للذوبان فى الماء ويسهل امتصاصة بالجسم وتستخدم بنزوات الصوديوم 0.1 % مم فى معظم الاغذية المحفوظة كمادة
حافظة لانها تمنع نمو الفطريات على الاغذية
حمض السيتريك
H - C- COOH H
HO-C-COOH
H -C- COOH
H يوجد فى الموالح مثل الليمون بنسبة 5-7 % والبرتقال بنسبة 1 % يمنع نمو البيكتريا على الاغذية لانة يقلل الرقم الهيدروجينى يضاف على الفاكهة المجمدة ليحافظ على لونها وطعمها
حمض الاسكوربيك
يوجد فى الحمضيات (الموالح) والفواكهة والخضروات مثل الفلفل الاخضر
-يتحلل بالحرارة وفعل الهواء -نقصة يؤدى إلى تدهور بعض الوظائف الحيوية فى الجسم والاصابة بمرض الإسقربوط
حمض السلسيلك
وهو من الفيتامينات التى يحتاجها الجسم بكمية قليلة
-تصنع منة كثير من مستحضرات التجميل الخاصة بالجلد لاعطائة النعومة او للحماية من اشعة الشمس كما
-استخدم منذ عام 1829 فى علاج امراض البرد والصداع قبل اكتشاف الأسبرين الا انة كان المتسبب فى قرحة المعدة
حمض لاكتيك C3H6O3 البن الذبادى – ينتج فى العضلات اثناء بذل مجهود كبير ويسبب الم كبير جدا
علل يحول حمض البنزويك إلى الملح الصوديومى او البوتاسيومىعند استخدامة
لانة غير قابل للذوبان فى الماء فيحول إلى الملح الصوديومى او البوتاسيومى ليكون قابل الذوبان
الاحماض الامينية
- الوحدة الأساسية التى يتكون منها البروتين
- مشتقات للأحماض العضوية حيث يتكون الحمض الأمينى من إحلال مجموعة امينو محل ذرة هيدروجين من مجموعة الألكيل الموجودة فى جزىء الحمض الكربوكسيلى (العضوى )
- NH2 + H-CH2 COOH NH2CH2COOH
حمض الجلايسين حمض امينو اسيتيك حمض الأسيتيك مجموعة امينو
-الأحماض الأمينية الموجودة فى الطبيعة متعددة
- يوجد منها 20 حمض أميني فقط فى البروتينيات الطبيعية
-الأحماض الأمينية الموجودة فى البروتينيات من النوع ألفا امينو أى تكون مجموعة الأمينو متصلة بالكربون فى الوضع ألفا وهى ذرة الكربون التى تلي مجموعة الكربوكسيل مباشرة
امثلة للاحماض الامينية
*حمض الأمينو اسيتيك
ابسط أنواع الأحماض الأمينية ويعرف بحمض الجلايسينNH2CH2COOH
*حمض الآلانين ويعرف بحمض امينو بروبانويك CH3-CH-COOH
NH2
البروتينات
- تعتبر البروتينات بوليمرات للاحماض الامينية
- جزىء الانسولين نجد ان كتلتة الجزيئية تبلغ 6000 وهو يتكون من 51 جزىء لستة عشر حمض امينى
- قد تصل الكتلة الجزيئية لبعض جزيئات البروتينات إلى اكثر من مليون كما فى الانزيمات المعقدة
يتبع






 اقتباس
اقتباس